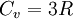Закон Дюлонга-Пти (Закон постоянства теплоёмкости) — эмпирический закон, согласно которому молярная теплоёмкость твёрдых тел при комнатной температуре близка к 3R:
где R — универсальная газовая постоянная.
Закон выводится в предположении, что кристаллическая решетка тела состоит из атомов, каждый из которых совершает гармонические колебания в трех направлениях, определяемыми структурой решетки, причем колебания по различным направлениям абсолютно независимы друг от друга. При этом получается, что каждый атом представляет три осциллятора с энергией E, определяемой следующей формулой:
 .
.
Формула вытекает из теоремы о равнораспределении энергии по степеням свободы. Так как каждый осциллятор имеет одну степень свободы, то его средняя кинетическая энергия равна  , а так как колебания происходят гармонически, то средняя потенциальная энергия равна средней кинетической, а полная энергия - соответственно их сумме. Число осцилляторов в одном моле вещества составляет
, а так как колебания происходят гармонически, то средняя потенциальная энергия равна средней кинетической, а полная энергия - соответственно их сумме. Число осцилляторов в одном моле вещества составляет  , их суммарная энергия численно равна теплоемкости тела - отсюда и вытекает закон Дюлонга-Пти.
, их суммарная энергия численно равна теплоемкости тела - отсюда и вытекает закон Дюлонга-Пти.
Приведем таблицу экспериментальных значений теплоемкости ряда химических элементов для нормальных температур:
| Элемент| | Cv , кал/(К·моль)| |
Элемент| | Cv , кал/(К·моль) | |
|---|---|---|---|---|
| C |
1,44 | Pt | 6,11 | |
| B | 2,44 | Au | 5,99 | |
| Al | 5,51 | Pb | 5,94 | |
| Ca | 5,60 | U | 6,47 | |
| Ag | 6,11 | - | - |
Зависимость теплоёмкости от температуры при низких температурах объясняется в моделях Эйнштейна и Дебая.
Источники
- И. В. Савельев, Курс общей физики, том 1.
- Сивухин Д. В. Общий курс физики Т. II. Термодинамика и молекулярная физика.